Tanto
tuonò che piovve, verrebbe da dire. Un gruppo di ricercatori cinesi avrebbe,
per la prima volta, modificato geneticamente alcuni embrioni umani. Lo rivela uno
studio uscito il 18 aprile su Protein
& Cell.
Il paper riapre
l’acceso dibattito che, nelle ultime settimane, ha visto scontrarsi gran parte
della comunità scientifica: è giusto manipolare gli embrioni umani? Sulle
colonne di Science e Nature molti scienziati hanno espresso
la propria preoccupazione per questo tipo di manipolazione genetica,
considerandola uno strumento in grado di aprire le porte alla nascita di bambini
selezionati geneticamente. Una posizione non condivisa da tutti.
Numerosi altri ricercatori, infatti, suggeriscono di andare avanti sebbene con
le dovute cautele nell’interesse dei circa venti milioni di pazienti affetti da
malattie rare nella sola Europa che potrebbero guarire definitivamente
sottoponendosi alla tecnica del gene
editing.
Ma la ricerca del gruppo guidato da Junjiu Huang dell’Università di Guangzho non è l’unica novità importante su
questo argomento anche il direttore del NIH Francis
Collins ha deciso di prendere posizione in merito alla modificazione
genetica degli embrioni umani. Ma procediamo con ordine.
I
ricercatori cinesi, secondo quanto riferisce Nature, hanno testato la capacità del sistema CRISPR / Cas9 di
modificare il gene responsabile della β-talassemia in alcuni embrioni umani. Ma
come è andata?
Nello studio sono stati utilizzati 86 embrioni “di scarto” cioè
non impiantabili, ottenuti da un centro per la fertilità. Dei 71 embrioni
sopravvissuti, 54 sono stati testati geneticamente. Dai risultati è emerso che
solo 28 embrioni sono stati editati con successo e solo in un alcuni di questi
è avvenuta la sostituzione del materiale genetico. Allo stesso tempo però sono avvenute
mutazioni non intenzionali e questo ha fatto scattare un campanello di allarme:
la tecnica non è ancora sicura.
Il team di Huang
ha rilevato un sorprendente numero di mutazioni “fuori bersaglio”. I tassi di queste
mutazioni erano molto più elevate di quelli osservate negli studi di gene-editing fatti su embrioni di topo o
in cellule adulte umane. Ed è lo stesso Huang ad ammettere le difficoltà: “Se
si vogliono ottenere degli embrioni normali, è necessario essere vicini al 100%
della sostituzione tra il gene funzionale e quello difettoso. Inoltre, aggiunge
il ricercatore, le mutazioni riscontrate sono forse inferiori a quelle che
avremmo potuto ottenere, questo perché abbiamo lavorato solo sulla porzione di
DNA definita exome. Tuttavia – continua
Huang – il nostro studio è molto importante perché dimostra, attraverso dei
dati, quello che potrebbe accadere applicando questa tecnica”.
Sull’importanza
dello studio non sono concordi i redattori di Nature e Science che,
secondo lo scienziato cinese, hanno rifiutato di prendere in esame il lavoro per
implicazioni etiche.
A proposito della rivista che ha accettato di pubblicare la ricerca si può notare
un particolare curioso: se si va sul sito Protein
& Cell e si scarica il lavoro si può leggere che la redazione ha
ricevuto il lavoro il 30 marzo e ha deciso di pubblicarlo il 1 di aprile. Un
solo giorno per valutarlo? Un po’ pochino se si considera che di solito passa almeno
qualche settimana, per non dire mesi, prima che una rivista scientifica accetti
di pubblicare un lavoro. Insomma o siamo di fronti a dei revisori solerti e
celerissimi oppure Protein & Cell
ha voluto cavalcare il momento di dibattito in corso per fare uno scoop. "In
questa situazione insolita, la decisione editoriale di pubblicare questo studio
non deve essere vista come un avallo di questa pratica, né un incoraggiamento a
simili tentativi", ha spiegato in un editoriale Xiaoxue Zhang, caporedattore della rivista. Dibattito
che la pubblicazione del lavoro di Huang non ha fatto che riaccendere.
Rudolf Jaenisch, presidente dell’International
Society for Stem Cell Research ha detto che “è troppo
presto per applicare questa tecnologia alle cellule della linea germinale, in
test clinici e a ogni ricerca che coinvolga l'uso di embrioni umani. Dovrebbe
essere fatta con cura e in accordo a rigide linee guida etiche”. Gli fa eco George Daley, biologo presso la Harvard
Medical School di Boston. “Lo studio di Huang dovrebbe essere un monito severo
per qualsiasi professionista che pensa la tecnologia di gene editing applicata
agli embrioni umani sia pronta per passare all’applicazione clinica”. In questa vicenda quello che, forse, desta
più preoccupazione è la differenza che vi è di legislazione tra le varie
nazioni.
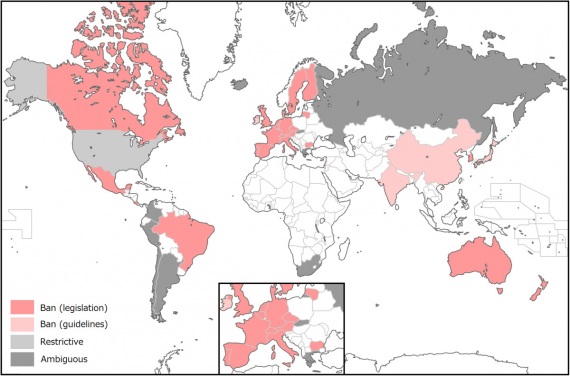
In uno
studio pubblicato nel 2014, Motoko Ishii
Araki e Tetsuya dell'Università
di Hokkaido, hanno esaminato le regole in 39 paesi e hanno scoperto che 29 di
loro (rosa più chiaro sulla mappa in basso) hanno un divieto su questo tipo di
ricerca. In Austria, ad esempio, "è vietato qualsiasi intervento che coinvolge la linea germinale umana."
Nel nostro Paese ci
sono leggi specifiche che vietano le manipolazioni sull’embrione e le cellule
germinali. In altre nazioni, come la Cina, non vi è nessuna regolamentazione o
quando è presente è alquanto ambigua. Ci sono delle linee guida che vietano la
pratica, ma la leggi non vengono applicate. E negli Stati Uniti? Dai due ricercatori giapponesi gli USA vengono
considerati come un “caso speciale”: no un totale divieto, ma delle le regole che sono molto restrittive.
Vi è una legge del 1996 conosciuta come l'emendamento Dickey-Wicker che vieta espressamente il finanziamento a questo tipo di ricerca. Ma per
fare chiarezza è intervenuto Francis Collins, direttore del NIH che
ribadito con fermezza il divieto da parte della sua Agenzia nel fare ricerca in
questo ambito.
La National
Institutes of Health è preoccupata per la sicurezza della tecnica e le
implicazioni etiche correlate.
Collins ha sottolineato il fatto che ci sono
poche situazioni cliniche in cui la modifica sarebbe l'unico modo per impedire
il passaggio di una malattia genetica da genitore a figlio. Secondo
Collins la questione della modifica embrioni è “una linea di ricerca che non
dovrebbe essere attraversata”.


