“Perché sono ancora così
pochi i medici che si fanno analizzare il DNA?” A chiederselo è George Church,
professore di genetica a Harvard, in un editoriale su Nature. “Non solo, ma dovremmo
fare molto di più - continua Church - per educare il pubblico ai benefici che
se ne potrebbero avere”. “E se cominciassi col farlo io?" mi chiedo. “E
se poi scopro che potrei ammalarmi di Alzheimer o di Parkinson o di certi
tumori cosa faccio?".
Comunque “meglio sapere”, penso tra me e me “o forse
no”.
Ne parlo in famiglia, mia moglie è un po’ preoccupata "sapere di cosa
morirai può cambiare la nostra vita"; i figli no, uno mi dice "sempre
meglio sapere, per te e un po’ anche per me", un altro "che bello lo
farei anch'io se fosse possibile", un'altra "papà se pensi di doverlo
fare va bene, ma se ci fossero cattive notizie non le voglio sapere".
Ma è
davvero così semplice farsi analizzare il DNA da noi? E quanto costa? E una
volta fatto il test chi lo interpreta? Devo ammettere di non avere le idee così
chiare. E allora cerchiamo di capire da dove è partito tutto e da quando l’uomo
ha cominciato a pensare che fosse possibile farsi analizzare il proprio DNA.
Il
26 giugno del 2000 Bill Clinton annuncia al mondo che la sequenza del genoma
(l'insieme di tutti i geni che stanno nel DNA del nucleo delle cellule) umano
era stata completata. Vicino a lui alla Casa Bianca quel giorno ci sono Francis
Collins e Craig Venter, i veri artefici di quel gigantesco sforzo. Passa
qualche anno e il primo a farsi sequenziale il suo DNA è proprio Francis
Collins. Era curioso di sapere di cosa si sarebbe ammalato ma soprattutto
voleva capire come funzionano le compagnie che creano e analizzano i dati. Sono
affidabili? Quanto tempo ci vuole per avere i risultati? E per interpretarli? E
chi lo fa? E quanto costa? Quello che ha fatto Collins l'hanno fatto ormai
migliaia di americani anche perché farsi sequenziare il genoma oggi costa 150
volte meno di allora. In Italia è tutto più complicato. Per cominciare,
l'analisi del DNA si può fare solo se c’è un dottore che certifichi che c'è una
ragione per farlo. Benissimo, sento il mio medico di famiglia: “Non so, non
saprei, non mi è mai successo che qualcuno volesse farsi analizzare il DNA”.
Parlo
con altri tre medici di base ma nessuno ha nessuna idea di quello che si
dovrebbe fare. Così faccio da solo. Compagnie che analizzano il DNA dell'uomo da
noi ce n'è almeno quattro: Genomnia a
Lainate, IGA Technology Services a Udine, BMR Genomics a Padova e Personal Genomics a Verona.
Di
solito si analizzano solo certe regioni del DNA, è per sapere che rischio c'è
di incorrere in una malattia che si è già manifestata in famiglia. Un'altra
possibilità è quella di farsi
sequenziare l'intero genoma. Scelgo questa seconda strada e mi rivolgo a
Personal Genomics a Verona. Il campione di sangue me lo prelevano il giorno del
mio compleanno, il tre aprile, nel mio Ospedale. Il DNA lo estraggono i miei
colleghi del Mario Negri (“è un buon DNA” mi dicono subito dopo l’estrazione, vuol
dire che la preparazione è venuta bene).
Poi il mio DNA va a Personal Genomics
e a metà maggio il sequenziamento è completo, adesso si tratta di interpretare
i risultati.
A Verona lo fanno in collaborazione con l’azienda americana Knome
e fanno anche di più, confrontano i loro dati con le piattaforme (così dicono i
genetisti) di due compagnie, Gentle a Lovanio e Genophen in California. Si
tratta di due approcci complementari. Ma prima di sbilanciarsi in qualunque
interpretazione tutti vogliono conoscere la mia storia e se sono stato malato e
di cosa, e poi vogliono informazioni sulla mia famiglia e sulle malattie dei
miei genitori; con Genophen è anche più complesso, si tratta di rispondere a un
questionario di quindici pagine in cui ti chiedono, malattie naturalmente, ma
anche abitudini alimentari, fumo, attività fisica e poi come e quanto dormi e
se sei nervoso almeno qualche volta e perché e cosa fai se sei nervoso e tanto
d’altro.
Ai primi di giugno arriva per email il “verdetto” di Knome e Gentle. Trovano
172 mila e 115 varianti nel mio genoma; è quello che mi rende diverso da 1000
altre persone apparentemente sane che sono lo standard di normalità.
Quindicimila e 459 di queste varianti sono piuttosto rare, le condivide con me solo il cinque
percento della popolazione. Di queste, 83 potrebbero darmi qualche problema più
in teoria che in pratica (sono varianti che indicano una predisposizione, la possibilità che un giorno
ti ammali davvero è estremamente remota).
Dieci di queste varianti però si trovano
in geni che hanno a che fare con certe malattie e questo si sa già.
Nel caso
mio c’è una variazione genica in eterozigosi - mi viene da uno solo dei
genitori - si tratta del gene MEF2A che attiva fattori di crescita delle
cellule e geni dello stress. Chi ha mutazioni di questo gene secondo uno studio
fatto negli Stati Uniti rischia di avere un infarto del cuore più degli altri.
Ci sono però almeno tre altri studi: uno fatto in Spagna, uno in Cina e uno a
Milano che non trovano nessun rapporto fra mutazioni di MEF2A e malattie del
cuore.
Così sono al punto di prima. So di avere una variante in un gene che
potrebbe predisporre a malattie del cuore, ma la cosa non è affatto sicura. Ho
un’altra variante in eterozigosi. E’ nel gene HFE che forma una proteina capace
di regolare assorbimento e deposito di ferro nei tessuti. Se la proteina non
funziona, il ferro si accumula nel fegato e questo dà origine a una malattia
che i medici chiamano emocromatosi, ma non è il mio caso. Se mai potrei essere
un portatore sano di una variante associata, ma solo in teoria, alla
predisposizione a quella malattia.
L’ultima variante è un gene che fornisce le
istruzioni per formare i canali del
calcio, strutture attraverso cui questo ione entra ed esce dalle cellule.
Saperlo serve a ben poco.
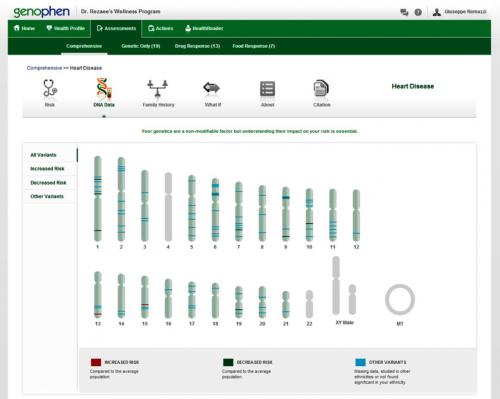
Intanto quelli dell’altra compagnia, Genophen, vanno avanti. La loro interpretazione del mio DNA si conclude entro la fine di giugno. “Risultato?” chiedo per email “Calma – mi dicono - prima dobbiamo organizzare una videoconferenza, parlerai con il nostro capo, Mehrdad Rezaee”. Fissiamo per il 18 luglio. Il collegamento dura più di un’ora. Rezaee ci tiene a premettere che il profilo di rischio per le malattie più comuni dipende soprattutto dalla storia familiare, dalle abitudini di vita, dall’alimentazione. Le variazioni del DNA potrebbero influire per il 20 percento, forse qualcosa di più, ma non sono certamente tutto. Giusto, ma a me interessa il DNA in questo momento. Ci concentriamo sul rischio cardiovascolare. Genophen trova nel mio DNA, insieme ad altre migliaia di varianti, due anomalie che si associano a un rischio aumentato di malattia coronarica, eccole lì le due varianti colorate in rosso sullo schermo dell'iPad.
 (ingrandisci l'immagine)
(ingrandisci l'immagine)
Legenda: La figura riporta
la distribuzione nei cromosomi del soggetto esaminato di diversi geni
che sono stati associati con il rischio di manifestare malattie
dell'apparato cardiovascolare. Nella figura sono evidenziate - con delle
lineette verde scuro - le varianti di alcuni geni sui cromosomi
1,6,7,9,10 e 19. Queste varianti sono state associate ad una riduzione
del rischio cardiovascolare. Nei cromosomi 13 e 15 sono evidenziate -
con lineette rosse - le varianti di due geni, che sono state invece
associate ad un aumento del rischio cardiovascolare. Le lineette azzurre
individuano varianti di geni di cui ancora non si conosce il ruolo nel
rischio vascolare, o che non sono state descritte nell'etnia caucasica.
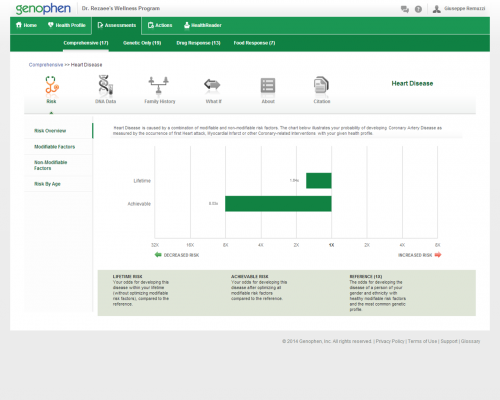
Comincio a preoccuparmi “con quella di Knome e Gentle sarebbero tre”. Ma la tabella successiva fa vedere che il mio rischio di infarto è inferiore alla media e potrebbe scendere ancora se mi muovessi di più e mangiassi più frutta e verdura. Non capisco, “e i tre geni ‘cattivi’ “?
 (ingrandisci l'immagine)
(ingrandisci l'immagine)
Legenda: Le malattie cardiovascolari risultano da una combinazione tra fattori di rischio che si possono modificare cambiando le abitudini alimentari e lo stile di vita e fattori di rischio non modificabili (genetici). Il grafico mostra la probabilità di sviluppare una malattia cardiovascolare nella persona in esame. Le barra orizzontale di colore verde in alto indica che il rischio complessivo è diminuito rispetto alla popolazione generale. Il numero accanto alla barra orizzontale indica di quante volte il rischio complessivo è inferiore alla media. La barra verde in basso indica di quanto ancora si potrebbe abbassare questo rischio agendo su abitudini alimentari e stile di vita.
Rezaee mi fa vedere un’altra figura, ci sono tutti i miei cromosomi e sopra ciascuno di loro diverse righette: rosse, verdi e azzurre, sono i geni che hanno a che fare con il rischio coronarico. A preoccupare sono i due rossi, ma ce ne sono nove verdi che invece proteggono dal rischio d’infarto. E i 72 azzurri? Non sono rilevanti per me, aumentano o diminuiscono il rischio di infarto in altre etnie (se uno è indiano per esempio o cinese).
Rezaee prima di appassionarsi di genetica era un cardiologo interventista. Gli chiedo se pensa che dovrei fare una coronarografia. Si mette a ridere. “Don’t go even close to a cardiologist” mi dice, insomma stai alla larga dai cardiologi. Rezaee va avanti, è un fiume in piena. C’è una quantità impressionante di tabelle e figure nel mio profilo. Vediamo: per l’aneurisma dell’aorta, per il cancro del colon e l’Alzheimer, per esempio, rischio meno della maggior parte delle persone ma rischio di più per calcoli della colecisti, osteoartrite e degenerazione maculare – una causa abbastanza comune di calo della vista - per adesso però ci vedo benissimo. Una curiosità: mia mamma è stata operata di colecisti qualche anno fa.
Sequenziare la parte
codificante del mio genoma è costato 1000 euro, ma per tutto quello che serve
per interpretare i dati si arriva come minimo a 3000 euro; costi proibitivi per
la gente, ma nei prossimi anni questi costi scenderanno e anche di molto. A
quel punto dovremo farla tutti l’analisi del DNA? Non è detto. Sapere che un
ragazzo potrà avere problemi di dipendenza dall’alcol o dalla nicotina o da
altre droghe può servire a proteggerlo, ma potrebbe anche succedere che la
predisposizione genetica diventi un alibi per non smettere.
Lo studio del Dna
cambierà quasi certamente il modo di fare medicina, le informazioni che ho io
adesso sul mio iPad relativamente al mio Dna ciascun medico potrebbe averle nel
suo computer per ciascuno dei suoi assistiti: “Signor Rossi lei sta benissimo
per adesso, ma il suo profilo genetico evidenzia un rischio aumentato di tumore
della prostata, si faccia vedere da un urologo almeno una volta all'anno”.
Questo però succederà solo quando i risultati dell'analisi del Dna saranno
completamente affidabili. Per ora non è così. E’ il caso di John – non è il suo
vero nome – che ha preso parte a uno studio del governo americano fatto per
verificare la validità di questi test e se vale davvero la pena di farli o no.
Aveva un’alterazione del ritmo del cuore per cui gli hanno impiantato un
pacemaker tredici anni fa.
Da allora il suo cuore funziona grazie agli impulsi
di quel piccolo apparecchio che si porta addosso. A John quattro compagnie
diverse hanno fatto sapere che in base al DNA rischia meno degli altri di avere
disturbi del ritmo del cuore, proprio il contrario di quello che invece gli è
successo. Per adesso lo studio del genoma ci ha insegnato soprattutto a
rivalutare la storia familiare, qualcosa che i medici stavano trascurando. Se
hai uno dei genitori malato di cuore, il rischio che tu ne soffra aumenta di
due volte e se uno dei tuoi parenti di primo grado ha avuto un cancro del colon
o della prostata o della mammella, rischi anche tu.
Quando ha deciso di farsi
analizzare il proprio DNA, Francis Collins grandi preoccupazioni non ne aveva
dato che i suoi genitori erano morti tutti e due a 98 anni. Il DNA ha confermato
che per le malattie più comuni Collins rischia meno della maggior
parte di noi, ha un rischio appena aumentato per diabete e degenerazione
maculare. Lui al DNA ci crede.
“Siamo preparati – si chiede alla
fine del suo libro The Language of Life –
a sapere quello che c’è da sapere del nostro DNA? E di quello dei nostri figli?
E di ciascun neonato al momento del parto?” Forse no. E forse non è
nemmeno così importante.
Approfondimento dell'articolo pubblicato su Il Corriere della Sera del 28-07-2014


